Lo reveló un estudio observacional del convupidiol, el primer producto con cannabidiol (CBD) aprobado en la Argentina de calidad farmacéutica y buenas prácticas de manufactura para el tratamiento de la epilepsia refractaria
Por años Argentina permaneció ajena a la aprobación de tratamientos a base de marihuana. La Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) ha sido conservadora respecto de los criterios para aprobar tratamientos en base a cannabidiol en el país. Sin embargo, cuando los científicos comenzaron a aportar investigaciones que reportaban las fortalezas de los medicamentos a base de esta sustancia, la entidad dio aprobación al primer producto con cannabidiol (CBD) de calidad farmacéutica y buenas prácticas de manufactura para el tratamiento de la epilepsia refractaria, focalizada en niños, del laboratorio Alef Medical Argentina.
Se trata del convupidiol, un medicamento recetado que se usa para tratar las convulsiones asociadas con el síndrome de Lennox-Gastaut o el síndrome de Dravet en personas de 2 años de edad y mayores. Ahora, desde la empresa dedicada la elaboración, compra, importación y venta de productos farmacéuticos publicaron los resultados del primer reporte preliminar de farmacovigilancia realizado en pacientes tratados con convupidiol a lo largo de 6 meses de tratamiento.
“Es importante destacar que este informe, realizado con el aporte de 13 colegas que brindaron información sobre 93 pacientes en tratamiento de epilepsia refractaria, es parte del compromiso asumido por Laboratorio Alef Medical con respecto a la seguridad de sus pacientes y como parte de un programa de Gestión de Riesgo aprobado por ANMAT”, escribieron en su informe los especialistas. Y añadieron: “Estamos complacidos de poder mostrarles estos primeros resultados, realmente alentadores, y esperamos poder seguir informando en siguientes entregas”.
La epilepsia es un cuadro neurológico que se manifiesta como consecuencia de una alteración en la actividad neuronal de alguna zona cerebral. Tiene una prevalencia que oscila entre el 4% al 10% por 1000 habitantes, es decir que aproximadamente una de cada cien personas lo padece. De ellas, el 30% presenta lo que se denomina “epilepsia refractaria” que engloba aquellos cuadros que no pueden controlarse con, al menos, dos de los fármacos antiepilépticos conocidos y en dosis adecuadas.
Para estos pacientes, el cannabis medicinal brinda una perspectiva alentadora y con resultados probados. “A partir de su administración, he notado en algunos pacientes la disminución en la frecuencia y la intensidad de las crisis”, explicó la doctora María Eugenia Sottano, neuróloga a cargo del área de Epilepsia Refractaria del Hospital Central de Mendoza.
A pesar de que en la actualidad se cuenta con más de 20 diferentes tipos de fármacos para la epilepsia, tal como cita un informe el CONICET, del 30 al 40% de los pacientes continúa teniendo crisis. Los datos preliminares de los estudios en humanos sugieren que el cannabis, en especial el cannabidiol, es efectivo en el tratamiento de algunos pacientes con epilepsia. Únicamente ensayos clínicos randomizados con estudios doble-ciego, placebo controlados, utilizando preparaciones farmacéuticas confiables y controladas de uno o más cannabinoides, brindarán información completa sobre la eficacia y seguridad de su uso. Para poder realizar estos ensayos resulta necesario contar con legislación que autorice el uso de cannabis en epilepsia.
Tal como alertó la médica británica Helen Cross, presidente de la Liga Internacional contra la Epilepsia, la calidad de los preparados es un punto fundamental. “Los aceites deben tener una elaboración correcta y una evaluación de sus compuestos”, declaró la especialista en el congreso internacional 2020 de la especialidad.
Ante la reglamentación sobre la ley de cannabis medicinal, distintas sociedades médicas nacionales publicaron un trabajo que analiza los conceptos sobre estos compuestos: “Existe una diferencia entre el cannabis farmacéutico de uso medicinal realizado por profesionales de la salud y atendiendo las buenas prácticas de manufactura, del preparado artesanal. Este último puede perseguir el objetivo de mejorar la calidad de vida, pero no cumple con los requisitos de eficacia que se requiere al hablar de un fármaco”.
“La distinción es siempre necesaria, aunque se torna crítica cuando se habla de situaciones de salud delicadas, como la epilepsia refractaria. Se han descubierto productos que no cuentan con los componentes que dicen tener. Otros donde, además del contenido, incluían sustancias tóxicas peligrosas”, concluyeron en una presentación conjunta la Liga Argentina de la Epilepsia, la Sociedad de Neurología Infantil, la Sociedad Argentina de Pediatría y la Sociedad Neurológica Argentina.
El cannabis farmacéutico asegura la estabilidad y homogeneidad de la molécula y cumple con todos los requisitos de seguridad y eficacia de cualquier fármaco registrado. La opción aprobada por el ANMAT es elaborada con buenas prácticas de manufactura, tiene certificados de calidad de producción y de materias primas y cuenta con la aprobación del Ministerio de Salud de la Nación. El mismo es de venta bajo receta archivada y, si bien se investigará su efecto en otras patologías, actualmente su uso es exclusivo para pacientes con epilepsia refractaria.
Considerando datos hasta febrero del 2022 se llevó adelante la recopilación de registros de pacientes con médicos prescriptores de convupidiol, quienes habían acordado brindar información clínica confidencial acerca del tratamiento de sus pacientes. El objetivo era el registro de la evolución de las frecuencias de convulsiones en sus pacientes. Para eso debían registrar las frecuencias de convulsiones al inicio del tratamiento y las frecuencias de convulsiones luego de 6 meses de tratamiento.
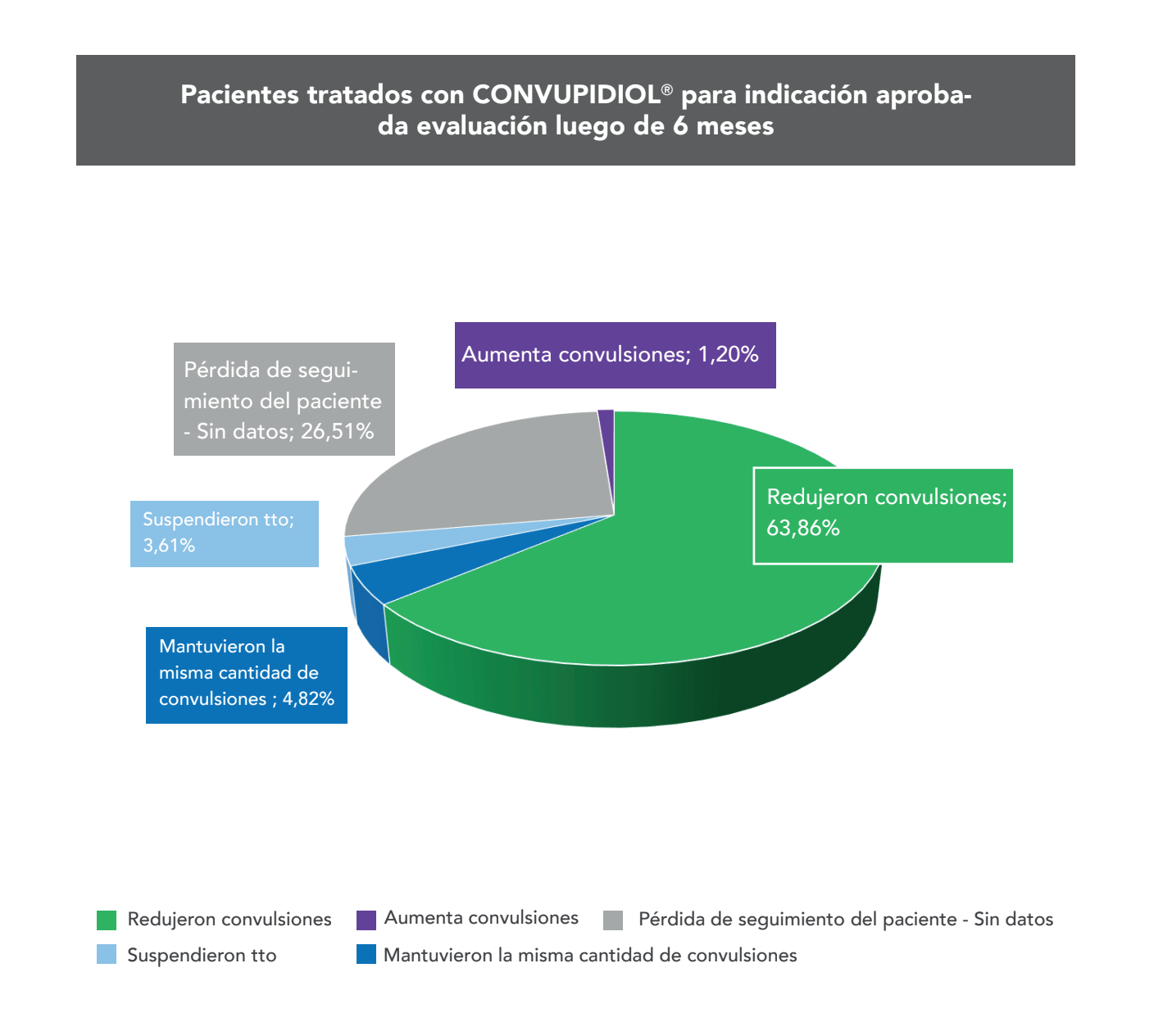
“Si consideramos solamente aquellos pacientes que fueron tratados con convupidiol para las indicaciones aprobadas en el prospecto y dejamos de lado los pacientes que recibieron el medicamento por una epilepsia no especificada en el prospecto, entonces se observa que un 63,86% de los pacientes redujeron sus convulsiones, 4,82% mantuvieron la misma cantidad de convulsiones, un 3,61% suspendieron el tratamiento, un 26,5% de los pacientes no asistieron a la visita de 6 meses y un solo paciente (que representa un 1,20% de la población evaluada) reportó aumento de las convulsiones”, detalla el estudio observacional.
Sin embargo, si se tienen en cuenta solamente los pacientes tratados con convupidiol para la indicación aprobada y que se presentaron a la visita de los 6 meses se observa que que un 87% redujo las convulsiones, un 7% mantuvo la misma cantidad de convulsiones, un 5% suspendió el tratamiento y un 2% aumentó las convulsiones. Y considerando solamente los pacientes que redujeron las convulsiones se analizó el promedio de reducción de convulsiones y se obtuvo un resultado promedio de 60,39% de reducción, con reducciones que variaban desde un 100% a un 17%.
Durante el período de investigación de datos se registraron 5 eventos adversos, 4 fueron eventos adversos no serios, y 10 fueron epilepsias no especificadas en el prospecto como la indicación aprobada. Según los especialistas, al momento de este informe recibieron un reporte inicial de un evento adverso serio. De los eventos adversos reportados “irritabilidad” y “diarrea” están listados en el prospecto del producto. En concreto, el perfil de seguridad demostró una cantidad esperada de eventos adversos principalmente no serios.
Analizando los datos recibidos se aprecia un claro efecto positivo en la menor cantidad de pacientes que presentan convulsiones al ser tratados con convupidiol luego de 6 meses(87% pacientes redujeron la cantidad de convulsiones al ser evaluados a los 6 meses). Aquellos pacientes que redujeron la cantidad de convulsiones presentaron una reducción promedio del 60,39%. “Este estudio de observación indica que en los casos de una buena adherencia al tratamiento y el seguimiento dedicado de los profesionales se observan resultados positivos para los pacientes mejorando su calidad de vida y la de sus familias”, concluyen.
Qué se sabe sobre los perfiles de seguridad de los medicamentos basados en cannabinoides
Los cannabinoides son una clase de medicamentos que son cada vez más reconocidos por las directrices nacionales y mundiales como posibles opciones de tratamiento para una variedad de afecciones. Se encuentran naturalmente en el cuerpo humano (endocannabinoides), se derivan de la planta de cannabis (fitocannabinoides) o se sintetizan en el laboratorio (cannabinoides sintéticos), según los hallazgos de una investigación publicada en la revista International Journal of General Medicine.
Aunque se han identificado aproximadamente 150 cannabinoides, los dos mejor estudiados son el tetrahidrocannabinol (THC) (responsable de los efectos eufóricos asociados con el cannabis) y el cannabidiol (CBD). Estos tienen diferentes propiedades farmacológicas y han demostrado eficacia en ensayos clínicos, ya sea solos o en combinación entre sí.
Si bien muchos estudios y revisiones de cannabinoides se centran en la eficacia, la seguridad se informa mucho menos. La evaluación general de la seguridad de los medicamentos a base de cannabinoides se confunde con el consumo de cannabis recreativo, así como con los diferentes diseños de estudios, indicaciones, dosificación y métodos de administración. Sin embargo, los estudios clínicos en productos registrados están cada vez más disponibles. Entonces, ¿qué se sabe hasta ahora sobre los perfiles de seguridad de los medicamentos basados en cannabinoides?
“En los últimos años, el interés creciente en los productos derivados del cannabis, en particular del CBD, se manifestó en el cambio de la legislación en numerosos países del mundo. La idea del cannabis de uso farmacéutico no debe estar disociada del uso farmacéutico de cualquier otra molécula. Esto implica evidencia médica de calidad y uso para indicaciones claras y precisas. También, implica que la elaboración sea realizada con las buenas prácticas de manufactura”, aseguró en el marco el webinar Farmacovigilancia en tratamientos con derivados del cannabidiol organizado por la Sociedad Argentina de Neurología Infantil (SANI), Patricia Saidón, médica especialista en Neurología y miembro del Comité Central de Ética en Investigación de la Ciudad de Buenos Aires.
Según advierte la Organización Mundial de la Salud (WHO, por sus siglas en inglés) en el informe CANNABIDIOL (CBD) Critical Review Report, “el cannabidiol (CBD) es uno de los cannabinoides naturales que se encuentran en las plantas de cannabis. Se trata de un compuesto terpenofenólico de 21 carbonos que se forma después de la descarboxilación de un precursor del ácido cannabidiólico, aunque también se puede producir sintéticamente. En los seres humanos, el CBD no presenta efectos indicativos de abuso o potencial de dependencia y se ha demostrado que es un tratamiento eficaz de la epilepsia en varios ensayos clínicos, con un producto de CBD puro con ensayos de Fase III completados y con revisión para su aprobación en los Estados Unidos. También hay evidencia preliminar de que el CBD puede ser un tratamiento útil para una serie de otras condiciones médicas”.
El concepto“cannabis medicinal”,como se lo suele entender tanto en las comunicaciones de prensa como en su uso coloquial, no implica hablar de una molécula químicamente pura, estable, sin la presencia de otros componentes y/o contaminantes, elaborada en torno a buenas prácticas de manufactura (BPM) que den cuenta de los distintos niveles de seguridad exigidos por los organismos regulatorios, tal cual sucede para cualquier otro fármaco.
“Es esta realidad lo que nos preocupa y nos lleva a la necesidad de aclarar las diferencias entre cannabis farmacéutico de uso medicinal -siempre realizado por profesionales de la salud y atendiendo a las BPM – del preparado artesanal, que puede perseguir el objetivo de mejorar la calidad de vida, pero que no cumple con los requisitos de seguridad y eficacia que se requiere al hablar de un fármaco. Dicha distinción es siempre necesaria, pero se torna crítica cuando se habla de patologías severas, como lo es la epilepsia resistente al tratamiento médico”, advirtieron ante la reciente propuesta de nueva reglamentación sobre la Ley de cannabis medicina, especialistas de la Liga Argentina Contra la Epilepsia (LACE), la Sociedad Argentina de Neurología Infantil (SANI), la Sociedad Argentina de Pediatría (SAP) y la Sociedad Neurología Argentina (SNA) en agosto de 2020.
Algunas de las exigencias de las buenas prácticas de manufactura son:contar con equipos destinados a la fabricación que estén calificados y con procesos validados, contar con personal capacitado y apropiadamente calificado para realizar los controles del proceso, poseer instalaciones, espacios y equipamientos apropiados, tener normatizados y escritos los procedimientos, rotular los materiales, envases y productos, los cuales deben ser trazables desde la elaboración hasta el almacenamiento y la entrega.
Fuente: Infobae
